Em 1900, o físico alemão Max Planck (1858-1947), em um trabalho sobre a radiação emitida por corpos aquecidos, conhecida como radiação de corpo negro, criou a teoria dos quanta ou teoria quântica, estabelecendo um novo conceito na física, o da quantização de energia.
Enquanto a física clássica trata de corpúsculos com distribuição contínua de energia, a física quântica abre espaço para a concepção de um mundo granular. Em substituição à visão contínua da natureza da matéria, introduz a ideia de que nem todos os valores de energia são possíveis, ou seja, a energia é quantizada e varia em quantidades denominadas “pacotes”, o que Plank chamou de quantum (daí o termo física quântica).
Mais tarde, essas unidades discretas de energia foram chamadas de fótons. Foi por meio dessas ideias que Einstein pôde explicar o efeito fotoelétrico, cujas aplicações são vastas na indústria moderna.

A Constante de Planck
Segundo Planck, a energia é quantizada, ou seja, não pode haver qualquer quantidade de energia, mas somente múltiplos de um valor mínimo fundamental. A menor quantidade de radiação de energia é o quantum. Um quantum de energia (E) é diretamente proporcional à frequência (f) da radiação:
E = h · f
Nessa expressão, h é uma constante denominada constante de Planck. No Sistema Internacional de Unidades (SI), a energia é medida em joules, a frequência é medida em hertz e a constante de Planck é medida em joule vezes segundo e seu valor é h = 6,63 · 10–34 J · s.
Como determinou Planck, a emissão ou absorção de energia só pode ocorrer em valores múltiplos de h · f; assim, a energia total emitida será:
E = n · h · f
Dessa forma, n é um número inteiro positivo (1, 2, 3, …) chamado de número quântico.
Exercício resolvido:
01. Qual o quantum de energia de um fóton de luz azul, cujo comprimento de onda é de 4.920 Å?
Resolução
Como 1 Å equivale a 10–10 m, o comprimento de onda dessa luz, em metros, vale:
λ = 4920 · 10–10 m = 4,92 · 10–7 m
Sabendo que a velocidade da luz é c = 3 · 108 m/s, temos que a frequência da luz azul é de:
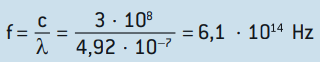
Calculando a energia de cada fóton pela constante de Planck, temos:
E = h · f
E = 6,63 · 10–34 · 6,1 · 1014
E = 4,04 · 10–19 J
Nota: por causa do valor muito pequeno da energia de um fóton, na física moderna, é muito comum utilizar a unidade de medida elétron-volt (eV) no lugar do joule (J).
1 eV = 1,6 · 10–19 J
Por: Daniel Alex Ramos