O estrôncio é um metal branco-prateado, macio, bom condutor de eletricidade. Quando exposto ao ar, oxida-se rapidamente e, por isso, deve ser conservado em querosene. Ao entrar em combustão no ar, produz uma luz brilhante e forma o óxido e o nitreto de estrôncio. Reage com a água e desse processo é formado o hidróxido de estrôncio e liberado o hidrogênio molecular.
É um elemento abundante na natureza: está presente, na forma de compostos de estrôncio, nas rochas magmáticas. Não é encontrado em sua forma metálica, mas especialmente na forma de sulfato de estrôncio.
As principais substâncias que contêm estrôncio são o carbonato de estrôncio (SrC03), o sulfato de estrôncio (SrS04), o hidróxido de estrôncio (Sr(OH)2) e o titanato de estrôncio (SrTi03).
Seu isótopo estável não apresenta perigo à saúde, mas os isótopos radioativos de estrôncio podem provocar câncer nos ossos.
O estrôncio não é produzido comercialmente.
É possível obtê-lo pela eletrólise de seu cloreto fundido e misturado ao cloreto de potássio, também em fusão, ou pela redução de seu óxido com o alumínio.

Aplicações
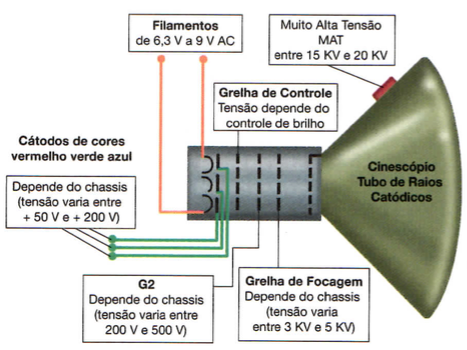
Uma das principais aplicações do estrôncio é a produção de cristais para cinescópios de televisores coloridos. É também usado na produção de ímãs de ferrita e na composição de ligas metálicas. O sulfeto de estrôncio é empregado na fabricação de tintas luminescentes. O titanato de estrôncio, por causa de seu elevado índice de refração, é utilizado na fabricação de materiais ópticos. Já o nitrato de estrôncio é empregado em pirotecnia, na produção de fogos de artifício.
Cerâmicas, vidros e pigmentos para pintura também podem conter o estrôncio. Substâncias que apresentam o isótopo estrôncio-90 são empregadas em radioterapia.

Nome do elemento: Strontium. Estrôncio
Origem do nome: Nome de uma cidade escocesa: Strontian.
Descobridor: Foi reconhecido pelo químico e físico escocês Adair Crawford (1748-1795), em 1790, e isolado pelo químico inglês Sir Humphry Davy (1778- -1829), em 1808.
Ano de descoberta: 1790
Número atômico (Z): 38
Massa atômica: 87,6200
Família: 2
Período: 5
Configuração eletrônica: [Kr]5s2
Raio atômico: 200 pm
Estado de agregação da substância simples (CNTP): sólido
TE (substância simples): 1 382 °C
TF (substância simples): 777 °C