O ferro puro é um metal branco-acinzentado, que na presença do oxigênio e do cloro assume a cor vermelha. Ele é capaz de decompor o vapor de água, liberando hidrogênio. Em pequena quantidade, o ferro não é tóxico.
É encontrado no Sol e em outras estrelas e é relativamente abundante na Terra, onde sua presença pode ser responsável pelo campo magnético do planeta.
Na forma de minérios, está presente em rochas e, na forma iônica, encontra-se em seres vivos, vegetais e animais, e em águas naturais.
Por ser magnético, o ferro é matéria-prima na fabricação de ímãs.
Quando submetido ao ar úmido, sofre oxidação, transformando-se em oxido de ferro, ou ferrugem. Para evitar a corrosão, é preciso revesti-lo por um metal que tenha mais facilidade em se oxidar do que ele. Quando revestido pelo zinco, é chamado de ferro galvanizado; quando revestido pelo crômio, recebe o nome de ferro cromado. O revestimento com estanho é chamado folha-de-flandres.

O ferro apresenta-se na natureza, geralmente, combinado ao oxigênio na forma de óxidos, como a hematita, mineral mais comum. A magnetita, a limonita, a pirita e a siderita são outros minérios de ferro.
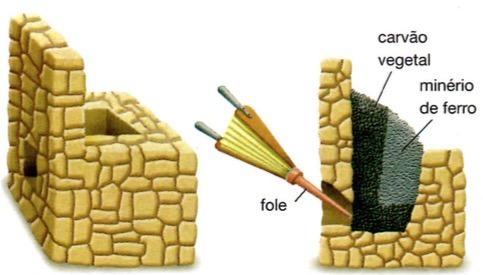
Para obter o ferro puro, a partir da hematita, é preciso eliminar o oxigênio do oxido. O processo mais comum para a obtenção do ferro é a redução do oxido com o carvão. Essa redução é feita em altos-fornos, nos quais são adicionados minérios de ferro, coque (carvão vegetal) e carbonato de cálcio, que atua como fundente, produzindo a escória. O ferro obtido em alto-forno tem o nome de ferro-gusa, ferro fundido ou simplesmente gusa.
As principais substâncias que contêm ferro são os óxidos de ferro (Fe203 e FeO), o sulfeto de ferro II (FeS), o sulfato de ferro II (FeS04) e o carbonato de ferro II (FeC03).
Aplicações
Desde tempos remotos, o ferro é conhecido e usado. Contas de ferro foram encontradas no Egito por volta de 4000 a.C.
Na Caldeia, peças de artesanato de ferro apareceram em escavações na antiga cidade de Ur, e acredita-se que os chineses já utilizavam o metal por volta de 2200 a.C.
A Idade do Ferro, que teve início em 1200 a.C. e durou até a expansão romana pelo mediterrâneo ocidental, marcou o último estágio cultural e tecnológico da Pré-História, em que o metal substituiu o bronze na fabricação de utensílios e armas. A exploração de jazidas datam de 1500 a.C. no Oriente Médio. Do primeiro milênio da era cristã em diante, o ferro difundiu-se por toda a humanidade.
Na forma metálica, o ferro praticamente não é utilizado. O metal é empregado na forma de ligas, como o aço, que é uma liga de ferro e carbono, processada em siderúrgicas. A essa liga podem ser adicionados outros elementos, como manganês, níquel e crômio, que produzem vários tipos de aço. Por causa da sua dureza e do preço baixo, o ferro é empregado na fabricação de automóveis, barcos e componentes estruturais de edifícios.
O ferro pode ser usado ainda na produção de fios, de arames e de folhas laminares. O aço inoxidável é muito usado na fabricação de materiais de utensílios domésticos de cozinha e de banheiro.
O ferro também é empregado na fabricação de móveis e materiais de decoração. Portões, grades e postes de iluminação podem ser feitos de ferro fundido. Muitas ferramentas, pregos, parafusos e roscas têm como matéria-prima o ferro.
O sulfato ferroso é empregado em tinturaria e como fungicida. O oxalato ferroso é usado em reveladores fotográficos, e o nitrato e o cloreto de ferro são empregados como reagentes industriais.
Nos seres vivos, o ferro, na forma iônica, é um componente essencial. Ele forma a hemoglobina do sangue, responsável pelo transporte do gás oxigênio dos pulmões para o resto do corpo. A falta de ferro pode provocar anemia.



Nome do elemento: Ferrum. Ferro
Origem do nome: Do latim ferrum. A palavra “ferro” em inglês (iron) origina da palavra escandinava iam.
Descobridor É conhecido desde a Pré-História, mas se acredita ter sido descoberto por egípcios, em 4000 a.C. O metal dá nome à idade vinda após a Idade do Bronze – a Idade do Ferro.
Ano de descoberta: desconhecido
Número atômico (Z): 26
Massa atômica: 55,8450
Família: 8
Período: 4
Configuração eletrônica: [Ar]3d64s2
Raio atômico: 140 pm
Estado de agregação da substância simples (CNTP): sólido
TE (substância simples): 2861 °C
TF (substância simples): 1 538 °C