A descoberta do fenômeno da isomeria, na primeira metade do século XIX, mostrou que as propriedades das substâncias químicas não dependem unicamente de sua composição, mas também do arranjo espacial dos átomos dentro da molécula.
Isomeria é o fenômeno relacionado à existência de dois ou mais compostos químicos com fórmulas e pesos moleculares idênticos, mas propriedades diferentes. Por ser menos frequente nos compostos inorgânicos, é considerada uma qualidade própria das substâncias orgânicas. O grande número de combinações possíveis das longas cadeias de carbono favorece seu aparecimento.
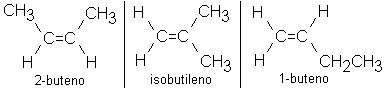
O conceito de isomeria envolve, portanto, aspectos relacionados com a posição dos átomos na molécula e a natureza das ligações atômicas. Um bom exemplo é o dado pela fórmula C4H8 que se refere de uma só vez a três compostos diferentes.
História
Os primeiros isômeros identificados foram o fulminato de prata, preparado em 1824 pelo químico alemão Justus von Liebig, e o cianato de prata, preparado no ano seguinte por Friedrich Wöhler. Verificando que as fórmulas das duas moléculas eram idênticas (AgCNO), concluiu-se que o arranjo espacial dos átomos era diferente.
Em 1830 o químico Berzelius observou que, na obtenção do ácido tartárico, originavam-se duas formas diferentes da mesma composição e formulou a primeira definição de isomeria, distinguindo-a da polimeria, que consiste no fenômeno da formação de substâncias compostas a partir da repetição de um determinado agrupamento chamado monômero.
Tipos de Isomeria
Foram descritos dois tipos de isomeria: a estrutural e a espacial.
A estrutural ou plana engloba todos os casos em que os isômeros são identificados por meio de suas fórmulas estruturais, com átomos ligados de maneira diferente. É classificada em isomeria de posição, de cadeia, de função e de compensação (metameria).
Já a espacial abrange os casos em que os isômeros só podem ser identificados pelo desenvolvimento de sua fórmula espacial. É dividida em isomeria ótica e geométrica (cis-trans).
Isomeria plana
A isomeria plana é comum entre todos os tipos de compostos orgânicos. Veja os casos mais comuns:
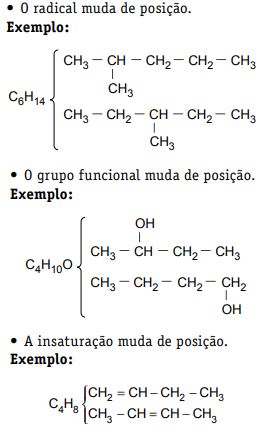
Isomeria de posição
Quando os isômeros pertencem à mesma função, possuem o mesmo tipo de cadeia carbônica, porém diferem quanto à posição relativa de um radical ligado à cadeia.
Isomeria de cadeia
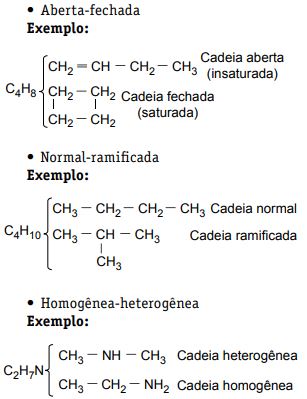
Quando os compostos pertencem à mesma função química, mas diferem quanto ao tipo de cadeia carbônica, diz-se que ocorre o fenômeno de isomeria de cadeia. As cadeias podem ser abertas ou fechadas, normais ou ramificadas e homogênea e heterogênea.
Isomeria de função
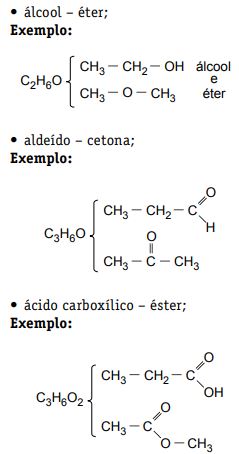
É chamada assim quando os compostos de mesma fórmula química possuem grupos funcionais diferentes. Pode ocorrer entre álcool e éter, aldeídos e cetonas e ácido carboxílico e éster.
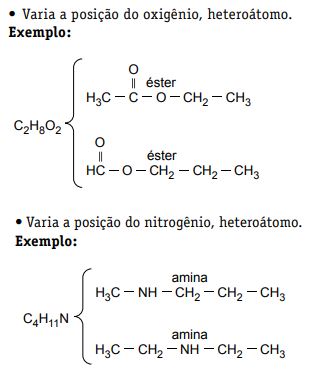
Isomeria de compensação (ou metameria)
Num caso particular, toma-se como referência a posição relativa de um heteroátomo ou de uma insaturação da cadeia. Os compostos de cadeia heterogênea, como os éteres ou ésteres, apresentam esse tipo de isomeria.
Tautomeria
Considerada um caso especial de isomeria de função, a tautomeria consiste no equilíbrio dinâmico entre dois isômeros. Um transforma-se no outro pela migração de um átomo de hidrogênio na molécula. 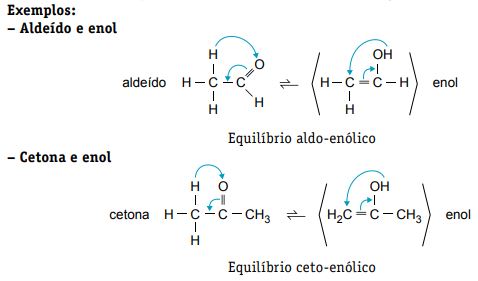
O fenômeno químico de transformação de um tautômero no outro recebe o nome de tautomerização, e a solução que contém as duas substâncias é chamada de mistura aleótropa. A tautomeria está dividida em desmotropina, na qual os tautômeros são isoláveis, e pseudomeria, quando não o são.
Isomeria Espacial
Isomeria espacial ou estereoisomeria é aquela em que isômeros apresentam fórmulas estruturais espaciais diferentes. Pode ser dividida em óptica e geométrica.
Isomeria óptica
Se os compostos têm a mesma fórmula estrutural e apresentam atividade óptica diferente (capacidade de desviar o plano da luz polarizada), a isomeria é denominada óptica.
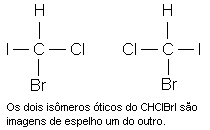
Os isômeros ópticos são pares de substâncias simétricas uma em relação à outra (como a mão direita e a esquerda). Cada uma delas gira o plano da luz polarizada num sentido. Esse fenômeno é característico dos compostos que apresentam um átomo de carbono assimétrico (ligado a quatro radicais ou átomos diferentes entre si).
As substâncias que desviam o plano da luz para a direita são chamadas de dextrógiras (representadas pelo sinal +) e as que desviam para a esquerda, levógiras (representadas pelo sinal -). A atividade óptica é a única propriedade física que diferencia esses compostos, chamados isômeros ópticos, enantiômeros ou antípodas ópticos.
Isomeria geométrica
Também conhecida como isomeria cis-trans, a geométrica ocorre em compostos em que há uma rigidez na estrutura molecular. Essa rigidez está quase sempre associada à presença de uma dupla ligação ou de anéis de átomos na substância.
Na maioria dos compostos em que dois carbonos estão ligados por uma dupla ligação, cada um deles também faz ligações simples com dois outros átomos (ou grupos de átomos), que podem diferir entre si. Os dois átomos de carbono e os quatro átomos, ou grupos de átomos, diretamente ligados a eles estão presos num mesmo plano pela dupla ligação.
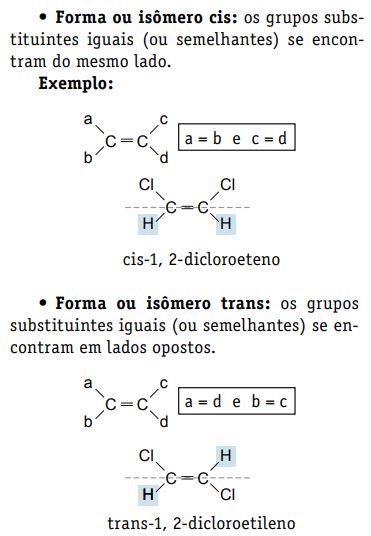
Existem portanto dois arranjos diferentes: um, chamado cis, em que os dois átomos ou grupos idênticos estão do mesmo lado da dupla ligação, e outro, chamado trans, em que estão em lados opostos.
Em cada par, o isômero cis difere do trans tanto física quanto quimicamente.
Para cada dupla ligação, podem existir dois isômeros geométricos. Quando há n duplas ligações, o número de isômeros geométricos possíveis é 2n.
Podem apresentar isomeria do tipo cis-trans todos os compostos com duplas ligações do tipo C=C ou C=X, ou ainda X=X, tendo X número de oxidação superior a 2, como o nitrogênio, por exemplo.
Em compostos cíclicos, pode-se considerar que o anel divide o espaço em dois planos. Assim, os radicais estão localizados no mesmo plano ou em planos opostos
Isômeros Geométricos
Como vimos no primeiro exemplo deste artigo, há três isômeros estruturais para o alceno C4H8. Você poderá ficar surpreso ao descobrir que existem, na realidade, quatro alcenos diferentes com esta fórmula molecular. O composto “extra” surge devido a um fenômeno denominado isomerismo geométrico. Veja os dois 2-butenos diferentes:
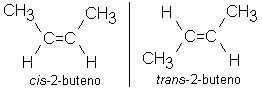
Resumindo
Isomeria é comum entre moléculas orgânicas. Os isômeros possuem a mesma fórmula molecular, porém diferem em suas estruturas e propriedades. Foram considerados na abordagem de isomeria nos compostos orgânicos dois tipos:
- Geométrica: cuja principal diferença entre os isômeros é quanto ao tipo de ligação entre os átomos.
- Óptica: cuja principal diferença entre os isômeros consiste em moléculas não-superponíveis
Por: Pedro Braz de Queiroz e Davi Fraga da Silva